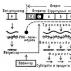
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Сущность процесса осмоса и его роль в биологических системах
Введение
1. Прямой осмос
1.1 Сущность процесса
1.2 Осмотическое давление
2. Механизм прямого осмоса в биологических системах
2.1 Структура биологической мембраны
2.2 Механизм прямого осмоса
3. Обратный осмос
Заключение
Список литературы
В ведение
Явление осмоса лежит в основе обмена веществ всех живых организмов. Благодаря ему в каждую живую клетку поступают питательные вещества и, наоборот, выводятся шлаки. Явление осмоса наблюдается, когда два соляных раствора с разными концентрациями разделены полупроницаемой мембраной.
В настоящее время мембранная технология является одной из самых динамично развивающихся областей технологии. Она получила широкое распространение, как на промышленном, так и на бытовом уровне.
Основной областью применения мембранной технологии является водоочистка и водоподготовка, однако ее применение не ограничивается этим.
В химической и нефтехимической промышленности мембранные методы разделения используются для разделения углеводородов, смесей высокомолекулярных и низкомолекулярных соединений, азеотропных смесей, смещения равновесия химических реакций путем удаления через мембрану одного из ее продуктов, концентрирование растворов, выделения гелия и водорода из природных газов, кислорода из воздуха и т.п.
В микробиологии и медицинской промышленности широкое применение мембранные методы находят в процессах выделения и очистки биологически активных веществ, вакцин, ферментов, гормонов, вирусов, очистки крови и решение других технологических задач.
Цель исследования - изучить сущность процесса осмоса и его роль в биологических системах.
1. Прямой осмос
1.1 С ущность процесса
Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ
Важным частным случаем осмоса является осмос через полупроницаемую мембрану.
Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя.
(Подвижность растворённых веществ в мембране стремится к нулю).
Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ.
Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (Рис. 1).
Рисунок 1. Прямой осмос
Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении.
Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда, как объём растворителя будет соответственно уменьшаться.
Например, к яичной скорлупе с внутренней стороны прилегает полупроницаемая мембрана: она пропускает молекулы воды и задерживает молекулы сахара. Если такой мембраной разделить растворы сахара с концентрацией 5 и 10 % соответственно, то через нее в обоих направлениях будут проходить только молекулы воды.
В результате в более разбавленном растворе концентрация сахара повысится, а в более концентрированном, наоборот, понизится. Когда концентрация сахара в обоих растворах станет одинаковой, наступит равновесие. Растворы, достигшие равновесия, называются изотоническими. Если принять меры, чтобы концентрации не менялись, осмотическое давление достигнет постоянной величины, когда обратный поток молекул воды сравняется с прямым.
Осмос, направленный внутрь ограниченного объёма жидкости, называется эндосмосом, наружу -- экзосмосом. Перенос растворителя через мембрану обусловлен осмотическим давлением.
Это осмотическое давление возникает соответственно Принципу Ле-Шателье из-за того, что система пытается выровнять концентрацию раствора в обеих средах, разделенных мембраной, и описывается вторым законом термодинамики.
Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса -- обратной диффузии растворителя.
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ, применяемый как способ очистки полимеров и коллоидных систем от низкомолекулярных примесей,
1.2 Осмотическое давление
Осмос можно объяснить тем, что концентрация молекул воды в единице объема в одном сосуде больше, чем в другом, или тем, что молекулы воды в растворе частично связываются молекулами сахара, гидратируя их. В разбавленных растворах осмос не зависит в явной форме от вида растворенного вещества и растворителя.
Решающее значение имеет концентрация раствора, точнее - число частиц растворенного вещества в единице объема.
Для исследования осмоса применяют специальный прибор (рис.2), состоящий из двух сосудов: внешнего и внутреннего.
Рисунок 2. Схематическое изображение прибора для исследования осмоса
Дно внутреннего сосуда изготавливают из полупроницаемой перегородки (пропускает растворитель, но не пропускает растворенное вещество, например целлофан).
В наружном сосуде - вода. Во внутреннем - раствор в воде. Из наружного сосуда вода будет переходить во внутренний. Во внутреннем сосуде ее уровень будет повышаться.
В результате повышается гидростатическое давление, под которым находится раствор во внутреннем сосуде. Вследствие этого скорость перехода воды из внутреннего сосуда во внешний возрастает. Наконец, при некоторой высоте столба раствора скорости прохождения воды из наружного сосуда во внутренний, и из внутреннего - в наружный сравняются, и подъем жидкости в трубке прекратится.
Давление, которое отвечает такому равновесию, может служить количественной характеристикой осмоса. Оно называется осмотическим давлением.
Осмотическим давлением называют давление, которое нужно приложить к раствору, чтобы привести его в равновесие с чистым растворителем, отделенным от него полупроницаемой перегородкой.
Анализируя результаты изучения осмотического давления, Я. Вант Гофф пришел к выводу, что растворенное вещество в очень разбавленных растворах ведет себя подобно тому, как если бы оно находилось в газообразном состоянии.
Отсюда возникла идея применения к ним законов идеальных газов. Тогда для раствора можно записать:
Заменяя n/V = с, получаем уравнение, названное законом Вант-Гоффа.
В этих уравнениях под п понимается осмотическое давление.
Линейная зависимость осмотического давления от концентрации для большинства растворов неэлектролитов сохраняется до концентраций порядка 10-2 моль/л.
Получим уравнение Вант-Гоффа исходя из термодинамических представлений. Растворитель будет проникать через полупроницаемую перегородку до тех пор, пока не установиться равновесие.
Уравнение Вант-Гоффа показывает, что осмотическое давление равно тому давлению, которое производило бы растворенное вещество, если бы оно в виде идеального газа занимало тот же объем, что и в растворе при той же температуре.
Осмотическое давление имеет очень большое значение в процессах жизнедеятельности различных организмов, определяя распределение растворенных веществ и воды в тканях. Осмотическое давление крови у человека составляет примерно 8.1 105 Па (8 атм.).
При уменьшении в организме содержания воды возникает чувство жажды, утоление которой восстанавливает водно-солевое равновесие и осмотическое давление крови.
От осмотического давления зависит, так называемая, сосущая сила клетки, достигая у семян при 6% влажности величины в 4.04 107 (400 атм.), что обеспечивает необходимое для прорастания поглощение воды даже из сравнительно сухой почвы.
Из (3) видно, что величина осмотического давления определяется лишь концентрацией растворенного вещества, и не зависит от природы раствора, что и позволяет отнести этот эффект к коллигативным свойствам.
Рассмотрим еще два свойства подобного рода: понижение точки замерзания (затвердевания) вещества и повышение температуры кипения.
Разность температур замерзания растворителя и раствора называют понижением точки замерзания.
Разность температур кипения раствора и растворителя называют повышением температуры кипения раствора Ткип.
Оба этих свойства находятся в полном согласии с принципом Ле-Шателье. Чтобы продемонстрировать сказанное, рассмотрим равновесную систему, состоящую из двух фаз: твердое вещество А и жидкий раствор вещества В, в котором А является растворителем.
Увеличим концентрацию раствора, т.е. содержание компонента В в жидкой фазе. Согласно принципу Ле-Шателье, в системе должны усилится процессы стремящиеся ослабить произведенное воздействие. В данном случае, это означает, что в системе должны усилится процессы, которые смогут уменьшить концентрацию раствора.
Для рассматриваемой системы, такое возможно лишь за счет перехода части растворителя из твердого состояния в жидкое. Однако, если при данной температуре происходит переход вещества из твердого состояния в жидкое, то эта температура выше точки замерзания. Следовательно, точка замерзания раствора при увеличении концентрации раствора понизилась.
Аналогично, исходя из принципа Ле-Шателье, можно обосновать повышение температуры кипения раствора нелетучего вещества.
Для этого рассмотрим двухфазную систему пар - жидкий раствор. Пусть система находится в равновесии; и пусть одна фаза представляет собой пар вещества А, а другая - жидкий раствор вещества В в А.
Увеличим концентрацию раствора (концентрацию В в А). Согласно принципу Ле-Шателье, это должно инициировать процессы, позволяющие нивелировать, произведенное увеличение концентрации.
Здесь к таким процессам относится конденсация растворителя из паровой фазы. Нетрудно понять, что конденсация приведет к понижению давления пара.
Понижение давления насыщенного пара повышает температуру кипения. Кипение жидкости наступает тогда, когда давление насыщенного пара над жидкостью сравнивается с внешним давлением.
Над раствором давление насыщенного пара понижается. Это означает, что для достижения указанного равенства давлений раствор необходимо дополнительно нагреть. Отсюда утверждение о повышении температуры кипения раствора в сравнении с чистым веществом.
Эффект повышения температуры кипения можно объяснить и иначе (рис.3).
Рисунок 3. Повышение температуры кипения
Действительно, в тех случаях, когда растворенное вещество имеет пренебрежимо малое давление пара, давление пара раствора равно давлению пара растворителя. Для идеальных растворов давление пара растворителя определяется законом Рауля:
где индексы «А» и «В» относятся к растворителю и растворенному веществу, соответственно.
Из (4) следует, что при возрастании хв давление насыщенного пара уменьшается, а значит, температура кипения возрастает.
Все сказанное демонстрирует рисунок, отражающий зависимость давления насыщенного пара над веществом от температуры.
Кипение наступает при равенстве давления насыщенного пара над жидкостью давлению внешнему (атмосферному).
Чтобы найти температуры кипения чистого растворителя и растворов, достаточно найти точки пересечения изобары при р = 1,013 10-5 Па с кривыми диаграммы состояния в координатах р - Т (см. рис.1). Из рисунка можно видеть, что раствор кипит при более высокой температуре, чем чистый растворитель.
осмос биологический мембрана диффузия
2. Механизм прямого осмоса в биологических системах
Формы связи влаги в этой системе играют существенную роль в формировании механизма прямого осмоса и фактически обусловливают полупроницаемость клеточной мембраны.
Классификацию форм связи влаги подобной двухфазной системы, разделённой биологической мембраной, рассмотрим с точки зрения классификации форм связи влаги, предложенной П.А. Ребиндером, которая позволяет учитывать как природу образования различных форм связи, так и энергию связи их с материалами.
В соответствии с точкой зрения этой классификации влагу, локализованную внутри дрожжевой клетки, необходимо рассматривать как осмотически удерживаемую влагу, обусловленную избирательной диффузией воды из окружающей среды. Осмотически удерживаемая влага характеризуется энергией связи слабой интенсивности, по своим свойствам не отличается от обычной воды и обладает способностью свободно диффундировать через клеточные мембраны под воздействием разности концентраций внутри и вне клеток.
К категории внутриклеточной влаги можно отнести и влагу, иммобилизованную в капиллярах клеточной стенки дрожжевой клетки - капиллярную влагу, которая играет существенную роль в механизме перераспределения влаги и фактически обусловливает полупроницаемость биомембраны.
Так, из анализа научной литературы известно, что влага, локализованная в капиллярах диаметром более 10-7 м (влага макрокапилляров), не имеет связи с материалом и может свободно перемещаться в процессе диффузии.
В свою очередь влага, локализованная в капиллярах диаметром менее 10-7 м (влага микрокапилляров) и обусловленная адсорбционной связью полимолекулярного слоя вблизи стенок капилляра, и не является свободной. Такая влага не участвует в диффузионных процессах ввиду особых свойств характерных для связанной влаги.
Как правило, адсорбционно-связанная влага, иммобилизованная на поверхности биомембраны в виде поверхностного мономолекулярного слоя адсорбированной воды (гидратной оболочки), также не участвует в процессах перераспределения влаги ввиду высоких значений энергии связи молекул воды с поверхностью биомембраны. Последующие слои адсорбционно-связанной жидкости (полимолекулярная адсорбция) удерживаются менее прочно и могут вовлекаться в диффузионные процессы.
Химически связанная влага не играет существенной роли в формировании механизма перераспределения влаги, поскольку количество её незначительно, а связи ионной и молекулярной природы очень прочны.
Таким образом, в формировании механизма прямого осмоса - перераспределения влаги через биомембрану дрожжевой клетки - участвуют осмотически удерживаемая влага, влага макрокапилляров, а также свободная избыточная внеклеточная влага, локализованная в межклеточном пространстве дрожжевой биомассы (рис. 4).
Рисунок 4. Формы связи влаги в дрожжевой клетке, локализованной в дрожжевой суспензии: 0 - химически связанная влага; 1 - осмотически удерживаемая влага (свободная внутриклеточная влага); 2 - свободная влага капилляров (влага макрокапилляров); 3 - связанная влага капилляров (влага микрокапилляров); 4 - адсорбционно-связанная влага; 5 - свободная внеклеточная влага (избыточная межклеточная влага)
2.1 С труктура биологической мембраны
Структура полупроницаемой клеточной мембраны дрожжевой клетки, представляющей собой капиллярно-пористое тело, играет ключевую роль в формировании механизма прямого осмоса - осмотически обусловленного самопроизвольного процесса перераспределения влаги из внутриклеточной среды дрожжевой клетки в межклеточное пространство при внесении в дрожжевую суспензию осмоиндуцирующего компонента (как правило, электролита).
Так, существенную роль в формировании механизма перераспределения играет система пор (капилляров) клеточной стенки биологической мембраны, которая является полупроницаемой, то есть низкоселективной для молекул воды и высокоселективной для гидратированных ионов осмоиндуцирующего компонента.
Исходя из представлений о строении растворов и результатов экспериментов, можно утверждать, что на селективность и проницаемость мембран влияет гидратирующая способность ионов.
Явление гидратации заключается в том, что ионы, растворного вещества окружены растворителем и движутся с некоторой его частью, вступающей с ним во взаимодействие.
При этом может наблюдаться как первичная, так и вторичная гидратация. Первичная гидратация заключается в прочном связывании ионов молекулы воды, вплоть до образования донорно-акцепторных связей. Вторичная - представляет собой электростатическое взаимодействие молекул воды с первично гидратированными ионами.
Молекулы воды, расположенные в непосредственной близости от ионов растворённых веществ, образуют гидратную оболочку, число молекул в которой характеризует координационное число гидратации.
Электростатическое взаимодействие не является единственной причиной гидратации - последняя может быть обусловлена и химическими силами.
Учитывая сказанное выше и основываясь на современных представлениях о связанной жидкости, процесс селективной проницаемости мембраны дрожжевой клетки по отношению к водным растворам электролитов можно представить следующим образом.
На поверхности и внутри пор (капилляров) клеточной мембраны дрожжевой клетки, локализованной в дрожжевой суспензии, возникает слой связанной воды. Вода на границе раздела фаз мембрана-раствор по своим свойствам отличается от воды в свободном состоянии. Например, связанная вода в значительной мере теряет растворяющую способность, поэтому наличие связанной воды в порах клеточной мембраны дрожжевой клетк одна из основных причин непроходимости для тех молекул растворённых веществ, для которых связанная вода практически не является растворителем. Если диаметр d пор мембраны d<2tc+dг.и. (где dг.и. - диаметр гидратированного иона), то через такую мембрану будет проходить только или преимущественно вода, что и обуславливает селективность (полупроницаемость) клеточной мембраны дрожжевой клетки.
Однако если для искусственных мембран, диаметр пор которых не превышает диаметра гидратированного иона, характерна 100 % селективность, то селективность биологических мембран никогда не достигает 100 %, так как реальные мембраны имеют поры различного диаметра (рис. 5), в том числе и крупные, превышающие величину 2tc+dг.и., а связанная вода хоть и в очень малых количествах все же обладает растворяющей способностью.
Рисунок 5. Схема механизма полупроницаемости биологических мембран
Таким образом, ключевую роль в формировании механизма прямого осмоса играет структура биологической мембраны дрожжевой клетки, полупроницаемость которой обусловлена:
1) наличием связанной воды в порах мембраны;
2) образованием в межклеточной фазе гидратированных ионов - крупных конгломератов ионов растворённого вещества с молекулами воды.
2.2 М еханизм прямого осмоса
Дрожжевая клетка, локализованная в дрожжевой суспензии, представляет собой систему, состоящую из двух фаз, разграниченных клеточной стенкой дрожжевой клетки - полупроницаемой мембраной.
При погружении в дрожжевую суспензию осмоиндуцирующего компонента, например хлорида натрия, происходит распад соли на множество микроскопических кристаллов.
Микрокристаллы, несущие в структуре своей кристаллической решётки как положительно заряженные ионы натрия, так и отрицательно заряженные ионы хлора, начинают испытывать силы ион-дипольного взаимодействия со стороны молекул воды. В процессе такого взаимодействия к положительно заряженным ионам натрия молекулы воды притягиваются своими отрицательными полюсами, а к отрицательно заряженным ионам хлора -положительными. Однако если ионы притягивают к себе молекулы воды, то и молекулы воды притягивают к себе ионы. В то же время притянутые молекулы воды испытывают толчки со стороны непритянутых молекул воды, находящихся в тепловом движении. Этих толчков, а также тепловых колебаний самих ионов оказывается достаточным для того, чтобы преодолеть силы, удерживающие ионы натрия или хлора в структуре кристаллической решётки монокристалла, и перевести их в раствор.
Вслед за первым слоем ионов в раствор переходит следующий слой и таким образом идет постепенное растворение микрокристалла. Перешедшие в раствор ионы остаются связанными с молекулами воды и образуют гидраты ионов, которые в значительной степени затрудняют обратную ассоциацию ионов с микрокристаллом. Таким образом, с физической точки зрения процесс растворения соли в дрожжевой суспензии фактически представляет собой процесс гидратации ионов осмоиндуцирующего компонента, сопровождающийся последующей его диссоциацией и образованием в растворе (межклеточной среде дрожжевой суспензии) множества ионов, окружённых гидратными оболочками (гидратированных ионов).
Поскольку биомембрана дрожжевой клетки является полунепроницаемой, компоненты рассматриваемой системы не являются изолированными друг от друга, поэтому при растворении соли в дрожжевой суспензии (погружении осмоиндуцирующего компонента в межклеточную среду дрожжевой суспензии) силы ион-дипольного взаимодействия между микрокристаллами и молекулами воды испытывают не только молекулы воды, находящиеся в межклеточном пространстве (фаза 1), но и молекулы воды, локализованные во внутриклеточном пространстве дрожжевой клетки (фаза 2).
Следовательно, можно предположить, что хаотичное тепловое движение молекул в результате взаимодействия молекул воды и ионов осмоиндуцирующего компонента, происходит во всей системе в направлении более высокой концентрации монокристаллов (более высокого химического потенциала), то есть наблюдается перераспределение влаги из внутриклеточной среды (фаза 1) в межклеточную среду (фаза 2).
Так как компоненты двухфазной системы не изолированы друг от друга, опираясь на вышеизложенные умозаключения, а также учитывая стремление любой системы к равновесию, было бы логичным предположить, что движение молекул воды в системе должно происходить и в обратном направлении, то есть из межклеточной среды во внутриклеточную. Однако подобного явления не наблюдается в силу особых свойств структуры клеточной мембраны и определённой специфики форм связи влаги в дрожжевой клетке, рассмотренных выше.
Гидратированные ионы, образовавшиеся в процессе ион-дипольного взаимодействия ионов осмоиндуцирующего компонента и молекул воды, являются достаточно крупными структурными образованиями и уже не могут покинуть межклеточное пространство (фазу 1). Таким образом, мы можем наблюдать ситуацию, когда число молекул воды, движущихся из фазы 1 в фазу 2, в значительной степени превалирует над числом молекул воды, движущихся в обратном направлении в силу того, что часть молекул воды, локализованных в межклеточном пространстве, не могут покинуть её в составе образовавшегося конгломерата иона осмоиндуцирующего компонента и воды (гидратированного иона).
При этом величина объёмного потока из фазы 2 в фазу 1 в значительной степени превалирует над величиной объемного потока в обратном направлении и в силу различной подвижности молекул воды и гидратированных ионов осмоиндуцирующего компонента, то есть фактически мы наблюдаем эффект перераспределения части внутриклеточной влаги в межклеточное пространство (рис. 6)
Подобный переход влаги через полупроницаемую мембрану дрожжевой клетки в межклеточное пространство будет продолжаться до тех пор пока:
а) в межклеточном пространстве дрожжевой суспензии будут присутствовать частицы способные оказывать влияние на процесс перераспределения, то есть вплоть до полной диссоциации осмоиндуцирующего компонента и образования максимально возможного числа гидратированных ионов (в случае низкой концентрации вносимого осмоиндуцирующего компонента);
б) присутствующие в системе молекулы воды будут обладать достаточной для иондипольного взаимодействия энергией и степенью свободы (в случае высокой концентрации вносимого осмоиндуцирующего компонента);
в) величина химического потенциала в межклеточной фазе в результате перераспределения влаги не достигнет минимально возможного показателя (в случае полного перераспределения влаги из внутриклеточного пространства в межклеточное).
Рисунок 6. Схема перераспределения внутриклеточной влаги в межклеточное пространство через полупроницаемую мембрану дрожжевой клетки при погружении в дрожжевую суспензию осмоиндуцирующего компонента
Следствием подобного перераспределения влаги является постепенное возникновение градиента давления - осмотического давления, приводящего к физической деформации клеточной стенки дрожжевой клетки и её сжатию - плазмолизу (рис. 7).
Рисунок 7. Изменение формы и размера дрожжевой клетки при погружении в дрожжевую суспензию осмоиндуцирующего компонента
Погружение осмоиндуцирующего компонента непосредственно в дрожжевую суспензию позволяет создать условия для индуцирования в системе максимально возможного числа частиц способных оказывать влияние на процесс перераспределения, а следовательно, обеспечить максимальную эффективность осмотического процесса. В тоже время погружение дрожжевой суспензии в готовый раствор осмоиндуцирующего компонента даёт минимальный осмотический эффект ввиду отсутствия в готовом растворе частиц способных оказывать влияние на процесс перераспределения, то есть если в первом случае процесс перераспределения влаги в биологической системе формируется за счёт совокупного эффекта концентрационного электроосмоса и капиллярного осмоса, то во втором - исключительно за счёт эффекта концентрационного электроосмоса.
Рассмотренная капиллярно-фильтрационная модель перераспределения влаги через полупроницаемую мембрану фактически отображает физическую модель явления прямого осмоса и позволяет достаточно детально представить процессы, происходящие как внутри, так и вне дрожжевой клетки в процессе перераспределения, а также объяснить природу самого явления.
3 . Обратный осмос
В случае, когда на раствор с большей концентрацией воздействует внешнее давление, превышающее осмотическое, молекулы воды начнут двигаться через полупроницаемую мембрану в обратном направлении, то есть из более концентрированного раствора в менее концентрированный. Этот процесс называется "обратным осмосом". По этому принципу и работают все мембраны обратного осмоса.
В процессе обратного осмоса вода и растворенные в ней вещества разделяются на молекулярном уровне, при этом с одной стороны мембраны накапливается практически идеально чистая вода, а все загрязнения остаются по другую ее сторону.
Рисунок 8. Обратный осмос
Таким образом, обратный осмос обеспечивает гораздо более высокую степень очистки, чем большинство традиционных методов фильтрации, основанных на фильтрации механических частиц и адсорбции ряда веществ с помощью активированного угля.
В системах обратного осмоса бытового назначения давление входной воды на мембрану соответствует давлению воды в трубопроводе. В случае, если давление возрастает, поток воды через мембрану также возрастает.
На практике, мембрана не полностью задерживает растворенные в воде вещества. Они проникают через мембрану, но в ничтожно малых количествах. Поэтому очищенная вода все-таки содержит незначительное количество растворенных веществ. Важно, что повышение давления на входе не приводит к росту содержания солей в воде после мембраны. Наоборот, большее давление воды не только увеличивает производительность мембраны, но и улучшает качество очистки. Другими словами, чем выше давление воды на мембране, тем больше чистой воды лучшего качества можно получить.
В процессе очищения воды концентрация солей со стороны входа возрастает, из-за чего мембрана может засориться и перестать работать. Для предотвращения этого вдоль мембраны создается принудительный поток воды, смывающий "рассол" в дренаж.
Эффективность процесса обратного осмоса в отношении различных примесей и растворенных веществ зависит от ряда факторов. Давление, температура, уровень pH, материал, из которого изготовлена мембрана, и химический состав входной воды, влияют на эффективность работы систем обратного осмоса.
Неорганические вещества очень хорошо отделяются обратноосмотической мембраной. В зависимости от типа применяемой мембраны (ацетатцеллюлозная или тонкопленочная композитная) степень очистки составляет по большинству неорганических элементов 85%-98%.
Мембрана обратного осмоса также удаляет из воды и органические вещества. Органические вещества с молекулярным весом более 100-200 удаляются полностью; а с меньшим - могут проникать через мембрану в незначительных количествах. Большой размер вирусов и бактерий практически исключает вероятность их проникновения через мембрану.
В то же время, мембрана пропускает растворенные в воде кислород и другие газы, определяющие ее вкус. В результате, на выходе системы обратного осмоса получается свежая, вкусная, настолько чистая вода, что она, строго говоря, даже не требует кипячения.
Заключение
Осмос играет важную роль во многих биологических процессах.
Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема.
Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию. Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур.
Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высокоминерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводные простейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддерживания постоянной концентрации растворимых в ней веществ. Осмос также играет большую роль в экологии водоёмов.
Список литературы
1. Дытнерский, Ю.И. Обратный осмос и ультрафильтрация / Ю. И. Дытнерский - М.: Химия, 1978. - 352 с
2. Латыпов, И.А. Исследование механизма самопроизвольных осмотических процессов массопереноса в системах биологического происхождения / И.А. Латыпов, М.К. Герасимов // ВестникКазан. технол. ун-та. - 2008. - №3. - С.85-91
3. Муштаев, В.И. Сушка дисперсных материалов / В.И. Муштаев, В.М. Ульянов - М.: Химия, 1988. - 351 с.
4. Уильямс, В. Физическая химия для биологов / В. Уильямс, Х. Уильямс. - М.:Мир, 1976. - 600 с.
5. Чураев, Н.В. Физикохимия процессов массопереноса в пористых телах / Н.В. Чураев - М.: Химия, 1990. - 271 с.
Размещено на Allbest.ru
Подобные документы
Принцип детального равновесия. Детерминизм классической механики. Броуновское движение молекул. Интегрирование уравнения Ланжевена. Коэффициент диффузии мембраны. Ориентация молекул по разные стороны от мембраны. Модель жидкокристаллического осмоса.
статья , добавлен 23.06.2012
Пассивный и активный транспорт веществ через мембранные структуры. Транспорт неэлектролитов путем простой и облегченной диффузии. Пассивный перенос неэлектолитов через биомембраны, уравнение Рика. Молекулярный механизм активного транспорта ионов.
курсовая работа , добавлен 25.02.2011
История открытия физического явления диффузия. Экспериментальное определение постоянных Больцмана и Авогадро. Закономерности броуновского движения. Схема диффузии через полупроницаемую мембрану. Применение физического явления диффузия в жизни человека.
реферат , добавлен 21.05.2012
Определение плотности потока формамида через плазматическую мембрану Chara ceratophylla толщиной 8 нм. Расчет коэффициента проницаемости плазматической мембраны Mycoplasma для формамида. Уравнение Фика для диффузии. Расчет потенциала Нернста для ионов.
контрольная работа , добавлен 09.01.2015
Ионная природа мембранных потенциалов. Потенциал покоя, уравнение Нернста. Стационарный потенциал Гольдмана-Ходжкина. Уравнение электродиффузии ионов через мембрану в приближении однородного поля. Механизм генерации и распространения потенциала действия.
реферат , добавлен 16.12.2015
Раздел физики низких температур, изучающий закономерности изменения свойств веществ в условиях криогенных температур. Рабочее тело в криогенных системах. Восстановление биологических функций после размораживания. Температура конденсации природного газа.
презентация , добавлен 10.08.2013
Определение теплоты сгорания топлива, объемов продуктов сгорания. Определение коэффициента теплоотдачи в теплообменнике. Уравнение теплового баланса для контактного теплообменника. Подбор и расчет газогорелочных устройств в системах теплогазоснабжения.
курсовая работа , добавлен 07.04.2015
Сканирующий туннельный микроскоп, применение. Принцип действия атомного силового микроскопа. Исследование биологических объектов – макромолекул (в том числе и молекул ДНК), вирусов и других биологических структур методом атомно-силовой микроскопии.
курсовая работа , добавлен 28.04.2014
Расчет профиля диффузии сурьмы в кремнии, определение основных параметров этого процесса. Использование феноменологической модели диффузии. Влияние параметров на глубину залегания примеси. Численное решение уравнения диффузии по неявной разностной схеме.
курсовая работа , добавлен 28.08.2010
Описание экспериментальной установки, принцип измерения давления воздуха и определение его оптимального значения. Составление журнала наблюдения и анализ полученных данных. Вычисление барометрического давления аналитическим и графическим методом.
История
Впервые осмос наблюдал А. Нолле в , однако исследование этого явления было начато спустя столетие.
Суть процесса
 Рис. 1.
Осмос через полупроницаемую мембрану. Частицы растворителя (синие) способны пересекать мембрану, частицы растворённого вещества (красные) - нет.
Рис. 1.
Осмос через полупроницаемую мембрану. Частицы растворителя (синие) способны пересекать мембрану, частицы растворённого вещества (красные) - нет.
Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану . Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. (Подвижность растворённых веществ в мембране стремится к нулю). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества (см. Рис. 1). Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём растворителя будет соответственно уменьшаться.
Например, к яичной скорлупе с внутренней стороны прилегает полупроницаемая мембрана: она пропускает молекулы воды и задерживает молекулы сахара . Если такой мембраной разделить растворы сахара с концентрацией 5 и 10 % соответственно, то через нее в обоих направлениях будут проходить только молекулы воды. В результате в более разбавленном растворе концентрация сахара повысится, а в более концентрированном, наоборот, понизится. Когда концентрация сахара в обоих растворах станет одинаковой, наступит равновесие. Растворы, достигшие равновесия, называются изотоническими . Если принять меры, чтобы концентрации не менялись, осмотическое давление достигнет постоянной величины, когда обратный поток молекул воды сравняется с прямым.
Осмос , направленный внутрь ограниченного объёма жидкости, называется эндосмосом , наружу - экзосмосом . Перенос растворителя через мембрану обусловлен осмотическим давлением . Это осмотическое давление возникает соответственно Принципу Ле Шателье из-за того, что система пытается выравнять концентрацию раствора в обоих средах, разделенных мембраной, и описывается вторым законом термодинамики. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса - обратной диффузии растворителя.
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ , применяемый как способ очистки полимеров и коллоидных систем от низкомолекулярных примесей, например электролитов .
Значение осмоса
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови , проницаема лишь для молекул воды, кислорода , некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко-минерализованной воды методом обратного осмоса жидкостей.
Клетки растений используют осмос также для увеличения объёма вакуоли , чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений). Пресноводные простейшие также имеют вакуоль, но задача вакуолей простейших заключается лишь в откачивании лишней воды из цитоплазмы для поддержания постоянной концентрации растворённых в ней веществ.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.
Использование в промышленности
Первая в мире электростанция - прототип, использующая для выработки электричества явление осмоса, запущена компанией Statkraft 24 ноября 2009 года в Норвегии вблизи города Тофте. Солёная морская и пресная вода на электростанции разделены мембраной ; так как концентрация солей в морской воде выше, между солёной водой моря и пресной водой фьорда развивается явление осмоса, - постоянный поток молекул воды через мембрану в сторону солёной воды. В результате чего давление солёной воды возрастает. Это давление соответствует давлению столба воды в 120 метров высотой, то есть достаточно высокому водопаду. Поток воды достаточен, чтобы приводить в действие гидротурбину, вырабатывающую энергию. Производство носит ограниченный характер, основная цель - тестирование оборудования. Самый проблематичный компонент электростанции - мембраны. По оценкам специалистов Statkraft мировое производство может составить от 1 600 до 1 700 TWh, что сравнимо с потреблением Китая в 2002. Ограничение связано с принципом действия - подобные электростанции могут быть построены только на морском побережье. Это не вечный двигатель, источником энергии является энергия солнца. Солнечное тепло отделяет воду от моря при испарении и посредством ветра переносит на сушу. Потенциальная энергия используется на гидроэлектростанциях , а химическая энергия долго оставалась без внимания.
Примечания
Ссылки
Wikimedia Foundation . 2010 .
Синонимы :Смотреть что такое "Осмос" в других словарях:
осмос - осмос, а … Русский орфографический словарь
ОСМОС, односторонняя диффузия РАСТВОРИТЕЛЯ (такого как вода) через естественную или искусственную полупроницаемую мембрану (перегородка, пропускающая только определенные растворенные вещества) в более концентрированный раствор. Из за того, что… … Научно-технический энциклопедический словарь
Свойство жидкостей соединяться, даже когда они разделены к. н. пористой перегородкой, также и самое это просачивание жидкостей. Полный словарь иностранных слов, вошедших в употребление в русском языке. Попов М., 1907. ОСМОС см. ЭНДОСМОС и… … Словарь иностранных слов русского языка
- (от греч. osmos толчок давление), односторонний перенос растворителя через полупроницаемую перегородку (мембрану), отделяющую раствор от чистого растворителя или раствора меньшей концентрации. Обусловлен стремлением системы к термодинамическому… … Большой Энциклопедический словарь
Осмоз Словарь русских синонимов. осмос сущ., кол во синонимов: 2 осмоз (1) электроосмос … Словарь синонимов
Осмос - (от греч. osmos толчок, давление) диффузия веществ в виде ионов через полупроницаемые клеточные мембраны. Осмос, направленный внутрь клеток, называется эндосмосом, наружу экзосмосом. Основной канал обмена веществ организмов с окружающей средой.… … Экологический словарь
осмос - – проникновение молекул растворителя через мембрану из растворителя в раствор или из раствора с меньшей концентрацией в раствор с большей концентрацией. Общая химия: учебник / А. В. Жолнин Осмос – диффузия растворителя через полупроницаемую… … Химические термины
- (от греческого osmos толчок, давление), самопроизвольный переход растворителя через полупроницаемую мембрану, не пропускающую растворённое вещество. Для того чтобы сохранить первоначальный состав раствора, необходимо приложить к раствору… … Современная энциклопедия
Государственное бюджетное образовательное учреждение высшего профессионального образования Волгоградский государственный медицинский университет Министерства Здравоохранения Российской Федерации.
Кафедра химии
Реферативная работа на тему:
«Коллигативные свойства растворов. Осмос и диффузия в растительной клетке»
Проверила: Складановская Наталия Николаевна
Подготовила:
студентка 2 курса
Игнатенко А.А
Фармацевтический факультет
202 группы
Волгоград 2015г
1.Введение
2. Коллигативные свойства.
3.Поступление воды в растительную клетку.
4. Диффузия.
6. Роль осмоса и осмотического давления в клетке.
7. Заключение.
8.Список литературы.
Введение
К коллигативным свойствам растворов, т.е. свойствам, зависящим от количества частиц, относятся осмотическое давление, диффузия, понижение температуры замерзания и повышение температуры кипения растворов по сравнению с чистым растворителем. Осмотическое давление обеспечивает упругость и эластичность тканей. Коллигативные свойства физиологических, гипертонических и гипотонических растворов связаны с их клиническими свойствами.
Осмос имеет большое значение в жизнедеятельности человека, животных и растительных организмов. Как известно, все биологические ткани состоят из клеток, внутри которых находится жидкость (цитоплазма), представляющая собой раствор различных веществ в Н2О. Оболочка клетки полупроницаема и через нее достаточно свободно проходит вода.
Снаружи клетки омываются межклеточной жидкостью, тоже представляющей собой водный раствор. Причем концентрация растворенных веществ внутри клеток больше чем в межклеточной жидкости. Вследствие осмоса наблюдается переход растворителя из внешней среды в клетку, что вызывает ее частичное набухание или тургор. При этом клетка приобретает соответствующую упругость и эластичность. Тургор способствует сохранению определенной формы органов у животных организмов, стеблей и листьев у растений. В срезанных растениях в результате испарения воды объем меж- и внутриклеточной жидкости уменьшается, снижается осмотическое давление, упругость клеток понижается и растение вянет. Увлажнение растений, помещение их в воду вызывает осмос и снова сообщает тканям упругость.
Коллигативные свойства.
Коллигативными свойствами называют растворы обладают рядом свойств, которые обусловлены общими причинами и определяются только концентрацией растворенного вещества, т.е., числом его частиц, молекул в системе, но не зависят от их массы, формы, размеров.
Такими свойствами являются:
Осмотическое давление,
Понижение давления насыщенного пара растворителя над раствором,
Повышение температуры кипения и понижение температуры замерзания раствора.
У растворов разных по своей природе веществ, но содержащих одно и то же число кинетически активных частиц растворенного вещества данные свойства будут одинаковые.
Это явление присуще разбавленным растворам нелетучих низкомолекулярных веществ, т.е., растворам, которые по своим характеристикам наиболее сильно приближаются к идеальным.
Поступление воды в растительную клетку.
Для осуществления всех процессов жизнедеятельности в клетку из внешней среды должны поступать вода и питательные вещества. Вода прямо или косвенно участвует во всех реакциях обмена и является важнейшей составной частью растительной клетки. Но помимо поступления воды в клетку может осуществляться и обратный процесс – выход воды из клетки. Эти явления объясняются процессами диффузии и осмоса.
Как известно, при температуре выше абсолютного нуля все молекулы находятся в постоянном беспорядочном движении. Это показывает, что они обладают определенной кинетической энергией. Благодаря постоянному движению при смешении двух жидкостей или двух газов их молекулы равномерно распределяются по всему доступному объему.
Диффузия.
Диффузия - это процесс, ведущий к равномерному распределению молекул растворенного вещества и растворителя. Как всякое движение, диффузия требует энергии. Диффузия всегда направлена от большей концентрации данного вещества к меньшей, от системы, обладающей большей свободной энергией к системе с меньшей свободной энергией.
Свободной энергией называется часть внутренней энергии системы, которая может быть превращена в работу. Свободная энергия, отнесенная к 1 молю вещества, носит название химического потенциала. А как известно химический потенциал можно определить как изменение любого вида энергии, сопровождающее изменение количества вещества в системе.
μi = (∂U/∂ni)S,V,nj = (∂H/∂ni)S,p,nj = (∂F/∂ni)T,V,nj = (∂G/∂ni)T,p,nj
где ni- число молей
индекс j ≠ i – постоянное количество всех dni компонентов, кроме ni.
Таким образом, химический потенциал - это мера энергии, которую данное вещество использует на реакции или движение. Химический потенциал - функция концентрации. Чем выше концентрация данного вещества, тем выше его активность и его химический потенциал.
Диффузионное передвижение вещества всегда идет от большего к меньшему химическому потенциалу. Так как химический потенциал характеризует способность рассматриваемого компонента к выходу из данной фазы или к выходу из данного состояния при химическом взаимодействии. В многофазных (гетерогенных) системах переход данного компонента может происходить самопроизвольно только из фазы, где его химический потенциал больше, в фазу, в которой его химический потенциал меньше. Поэтому переход сопровождается уменьшением химического потенциала компонента в 1-й фазе и увеличением во 2-й. В результате, разность между химическими потенциалами данного компонента в этих двух фазах уменьшается и при достижении равновесия химический компонента становится одинаковым в обеих фазах. В любой равновесной гетерогенной системе химический потенциал каждого компонента одинаков во всех фазах. Значит,в неравновесных системах любой компонент будет стремиться из состояния с более высоким химическим потенциалом в состояние с более низким потенциалом до тех пор, пока не установится равновесие.
Разность величин μ определяет направление химических реакций, фазовых превращений, диффузии веществ из одной фазы в другую. Добавление к воде молекул растворенного вещества приводит к возникновению связи между молекулами воды и растворенного вещества, что уменьшает ее активность, ее свободную энергию, ее химический потенциал. В том случае, если диффундирующие вещества встречают на своем пути мембрану, движение замедляется, а в некоторых случаях прекращается.
Скорость диффузии зависит от температуры, природы вещества, разности концентраций. Чем выше концентрация данного вещества, тем выше его активность и его химический потенциал.
Диффузия воды по направлению от большего к меньшему химическому потенциалу через мембрану носит название осмоса. Иначе говоря, осмос - это диффузия воды или другого растворителя через полупроницаемую перепонку, вызванная разностью концентраций или разностью химических потенциалов.
Осмос.
Осмос - результат неравенства химических потенциалов воды по разные стороны мембраны. Идеальная полупроницаемая мембрана пропускает молекулы воды и не пропускает молекулы растворенного вещества.
Одним из выдающихся ученых работавших в данной области был Вильгельм Пфеффер – немецкий ботаник и физиолог растений. Родился в Гребенштейне, близ Касселя. Изучал химию и фармацевтику в Гёттингенском университете (1863-1865). Основные работы посвящены физиологии растений. Изучал осмотические явления в растительных клетках, обусловливающие поглощение растениями воды и минеральных веществ. В эти работы Пфеффера заложены основы мембранной теории клеточной проницаемости. С помощью сконструированного им осмометра с полупроницаемой перегородкой из железосинеродистой меди (ячейка Пфеффера) установил (1877) зависимость осмотического давления от концентрации раствора, температуры и размера молекул, обобщённые Я. Г. Вант-Гоффом (1887). Исследовал процессы дыхания и азотного обмена в растениях, энергетику фотосинтеза, превращения запасных питательных веществ, физиологию раздражимости и механику движения листьев и цветков. Открыл положительный хемотаксис у гамет папоротников.
Как уже упоминалось выше В.Пфеффер в 1877 г. приготовил искусственную полупроницаемую мембрану. Для этого в пористый фарфоровый сосуд наливали раствор медного купороса и помещали в другой сосуд, заполненный раствором ферроцианида калия. В порах первого фарфорового сосуда растворы соприкасались и реагировали друг с другом. В результате в порах образовалась пленка из ферроцианида меди Cu 2 , которая обладала полупроницаемостью.
Таким образом, была создана модель клетки: полупроницаемая пленка имитировала мембрану, а стенки сосуда - пектоцеллюлозную оболочку. Сосуд, в порах которого образовалась полупроницаемая мембрана, заполненный раствором сахарозы, помещали в воду.
Такой прибор получил название осмометра.

Схема осмометра Пфеффера на Рис.1: 1 - сосуд с растворителем; 2- мембрана; 3 - ячейка с раствором; 4 - манометр.
Продолжив изучения, В. Пфеффер установил такой факт - поступление воды в раствор через полупроницаемую перегородку обусловливается разностью между свободной энергией чистой воды и раствора - данный процесс происходит самопроизвольно по градиенту свободной энергии воды. Кроме того, Пфеффер обнаружил, что химический состав раствора не изменяется после его разбавления, то есть пленка обладает селективностью (избирательностью) по проникающим компонентам. Так появился термин «полупроницаемая мембрана».

Схема эксперимента по измерению осмотического давления (Рис.2)
Однако Пфеффер не смог установить количественные зависимости осмотического давления от концентрации и температуры.
Данную зависимость вывел Вант-Гофф:
Линейная зависимость осмотического давления от концентрации раствора и от температуры соблюдается только для идеальных растворов. То есть уравнение для идеальных растворов имеет вид:
Поэтому уравнение можно применять только для разбавленных растворов. Если растворенное вещество диссоциирует и имеет степень диссоциации, то в простейшем случае диссоциации одной частицы на две имеем АВ-А+ + В-.
Число недиссоциированных частиц, получившихся из 1 моль, равно (1-а) моль, число продуктов диссоциации равно 2а моль, а всего молей будет 1 - а + 2а=1+a.
Сумму 1 +а обозначают буквой i. Это так называемый изотонический коэффициент Вант-Гоффа.
Тогда уравнение осмотического давления принимает вид
где π – осмотическое давление,
i – коэффициент Вант-Гоффа,
R – универсальная газовая постоянная, 8,31 Дж/моль∙К
T – абсолютная температура, К
Идеальными при любых концентрациях являются растворы, компоненты которых близки по физическим и химическим свойствам и образование которых не сопровождается объёмными и тепловыми эффектами. В этом случае силы межмолекулярного взаимодействия между однородными и разнородными частицами примерно одинаковы, и образование раствора обусловлено лишь энтропийным фактором.
Реальные растворы компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области бесконечно малых концентраций.
В осмометре при наличии полупроницаемой мембраны вода будет поступать в раствор, что приведет к его разбавлению, и движение воды будет замедляться.
Наступает термодинамическое равновесие. Термодинамическим равновесием называется такое термодинамическое состояние системы, которое при постоянстве внешних условий не изменяется во времени, причём, эта неизменяемость не обусловлена каким-либо внешним процессом. Таким образом, давление столба жидкости уравновесит силу, с которой молекулы воды поступают в осмометр. Энергия молекул воды, которая уменьшилась благодаря введению растворенного вещества, восполнится давлением столба жидкости. Это давление повышает химический потенциал раствора (μ р), делая его равным химическому потенциалу чистой воды (μ в). В этом период времени наблюдается осмотическое равновесие. Так как осмотическое равновесие было достигнуто процесс осмоса останавливается.
Если после достижения осмотического равновесия со стороны раствора приложить давление, превышающее осмотическое, то растворитель начнет переходить из раствора в обратном направлении. В этом случае будет иметь место обратный осмос.
Присоединив манометр, можно измерить давление, которое надо приложить к системе, чтобы предотвратить поступление воды в раствор и наоборот.
Обратный осмос применяется в фильтрующих установках для очистки и обогащения воды минералами.

Содержание статьи
ОСМОС, перенос вещества из одного раствора в другой через мембрану. Мембраны, проницаемые не для всех, а лишь для определенных веществ, называют полупроницаемыми. Например, к яичной скорлупе с внутренней стороны прилегает полупроницаемая мембрана: она пропускает молекулы воды и задерживает молекулы сахара. Если такой мембраной разделить растворы сахара с концентрацией 5 и 10% соответственно, то через нее в обоих направлениях будут проходить только молекулы воды. Поскольку вода будет перетекать из разбавленного раствора в концентрированный быстрее, чем в обратном направлении, в целом движение воды между двумя растворами будет идти в одну сторону. В результате в более разбавленном растворе концентрация сахара повысится, а в более концентрированном, наоборот, понизится. Когда концентрация сахара в обоих растворах станет одинаковой, наступит равновесие. Растворы, достигшие равновесия, называются изотоническими.
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода , растворенных в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворенном состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Как механизм осмоса, так и факторы, определяющие проницаемость мембран, еще не до конца изучены. Полупроницаема ли данная мембрана и если да, то для каких веществ, можно узнать только опытным путем.
Осмотическое давление.
Когда два раствора с разной концентрацией растворенных веществ разделены полупроницаемой мембраной, на нее действует сила, направленная от более разбавленного к более концентрированному раствору. Эта сила, называемая осмотическим давлением, может быть очень значительной. В дереве, например, под действием осмотического давления растительный сок поднимается от корней до самой верхушки. Но в дереве движение концентрированного раствора, каким является растительный сок, ничем не ограничено. Если же подобный раствор находится в замкнутом пространстве, например в клетке крови, то осмотическое давление может привести к разрыву клеточной стенки. Именно по этой причине лекарства, предназначенные для введения в кровь, растворяют в изотоническом растворе, содержащем столько хлорида натрия (столовой соли), сколько нужно, чтобы уравновесить осмотическое давление, создаваемое клеточной жидкостью. Если бы вливаемые лекарственные препараты были изготовлены на воде, осмотическое давление, заставляя воду проникать в клетки крови, приводило бы к их разрыву. Если же ввести в кровь слишком концентрированный раствор хлорида натрия, то вода из клеток будет выходить наружу, и они сожмутся.
Величина осмотического давления, создаваемая раствором, зависит от количества, а не от химической природы растворенных в нем веществ (или ионов, если молекулы вещества диссоциируют). Чем больше концентрация раствора, тем больше создаваемое им осмотическое давление. Это правило, носящее название закона осмотического давления, выражается простой формулой, очень похожей на закон идеального газа. Закон осмотического давления можно использовать для расчета молекулярной массы данного вещества.
Осмос имеет большое значение в жизнедеятельности человека, животных и растительных организмов. Как известно, все биологические ткани состоят из клеток, внутри которых находится жидкость (цитоплазма), представляющая собой раствор различных веществ в Н 2 О. Оболочка клетки полупроницаема и через нее достаточно свободно проходит вода.
Ионы электролитов и молекулы других веществ оболочка пропускает строго избирательно.
Снаружи клетки омываются межклеточной жидкостью, тоже представляющей собой водный раствор. Причем концентрация растворенных веществ внутри клеток больше чем в межклеточной жидкости. Вследствие осмоса наблюдается переход растворителя из внешней среды в клетку, что вызывает ее частичное набухание или тургор. При этом клетка приобретает соответствующую упругость и эластичность. Тургор способствует сохранению определенной формы органов у животных организмов, стеблей и листьев у растений. В срезанных растениях в результате испарения воды объем меж- и внутриклеточной жидкости уменьшается, снижается осмотическое давление, упругость клеток понижается и растение вянет. Увлажнение растений, помещение их в воду вызывает осмос и снова сообщает тканям упругость.
Кровь, лимфа, тканевые жидкости человека представляют собой водные растворы молекул и ионов многих веществ и обладают вследствие этого определенным осмотическим давлением. Причем на протяжении всей жизни организма биологические жидкости сохраняют свое давление на постоянном уровне независимо от состояния внешней среды. Это явление называется иначе изоосмией человеческого организма и является составной частью более общего процесса – гомеостаза или постоянства ряда физико-химических показателей внутренней среды человека в изменяющихся внешних условиях.
Изоосмия особенно присуща таким биологическим жидкостям как кровь и лимфа. Так осмотическое давление крови у человека практически постоянно и при 37 о С изменяется в пределах 740-780 кПа (т.е., почти в 8 раз больше атмосферного).
Осмотическое давление крови у разных живых организмов неодинаково. Так у лягушек оно ниже, чем у человека, а у некоторых морских животных, наоборот, больше.
При изменении осмотического давления крови организм стремится восстановить его, удалив из крови избыточное количество растворенных частиц (если давление повышается) или, наоборот, увеличивая число кинетически активных частиц (если давление понижается). Основную роль в регуляции осмотического давления крови играют почки. В меньшей степени в сохранении изоосмии участвуют ткани печени и подкожной клетчатки. Они способны накапливать избыточные количества солей. При поражении почек вклад подкожной клетчатки в поддержание осмотического давления резко увеличивается. Содержание солей в ее клетках возрастает, что приводит вследствие осмоса к значительному увеличению объема клеток и появлению отечности.
Изоосмия регулируется, прежде всего, центральной нервной системой и деятельностью желез внутренней секреции.
Отклонение осмотического давления крови от нормы вызывает болезненное состояние. Так при его понижении наблюдается рвота, судороги, затемнение сознания. Повышение осмотического давления сопровождается отечностью, нарушением сердечной деятельности.
В некоторых случаях изменение осмотического давления в ограниченных участках тканей могут быть довольно большими. Так при локальных воспалительных процессах белковые молекулы в клетках распадаются на массу более мелких фрагментов, увеличивая тем самым число растворенных частиц в них. Вода из окружающих тканей и сосудов устремляется в эти клетки и значительно увеличивает их объем. При этом в районе воспалительного очага возникает опухоль. При ее разрезе или проколе гнойная жидкость вытекает из нее под большим давлением.
Растворы, осмотическое давление которых равно осмотическому давлению раствора принятого за стандарт, называются изотоническими . В медицине осмотическое давление растворов сравнивают с осмотическим давлением крови. Изотоническими по отношению к крови являются 0,9% (0,15 М) растворNaClи 4,5-5% раствор глюкозы. В этих растворах концентрация частиц растворенного вещества такая же, как и в плазме крови. Отличие состоит лишь в том, что в состав крови входит не толькоNaClили глюкоза, но и целый ряд других веществ. Их суммарная концентрация носит названиеосмолярности (изотонической концентрации ) и представляет собой химическое количество всех кинетически активных (т.е., способных к самостоятельному движению) частиц (независимо от их формы, размеров и природы), содержащихся в 1 литре плазмы крови.
Осмолярная концентрация крови у человека составляет 0,287-0,303 моль/л.
Изотонические растворы NaClи глюкозы называют частофизиологическими растворами . Хотя в настоящее время этот термин для них признан неудачным, т.к. строго говоря, истинным физиологическим раствором является раствор по своему количественному и качественному составу максимально приближенный к плазме крови.
Растворы, обладающие более высоким осмотическим давлением, чем плазма крови, называются гипертоническими , а растворы, имеющие более низкое давление – гипотоническими .
При различных лечебных процедурах в кровь человека в больших количествах следует вводить только изотонические растворы, чтобы не вызвать осмотический конфликт из-за резкого несоответствия между осмотическим давлением биологической жидкости и вводимого раствора.
При контакте клетки с гипертоническим раствором происходит отток воды из клетки через мембрану в окружающую среду. Клетка при этом теряет свою упругость, вследствие обезвоживания и уменьшается в объеме (сморщивается). Нормальное течение физических и химических процессов в ней нарушается (рис. 25).

Рис. 25. Схематическое изображение процессов плазмолиза (а) и лизиса (б), протекающих в результате помещения клетки, соответственно, в гипертонический или гипотонический растворы.
Данное явление называется плазмолизом илиэкзосмосом .
Плазмолиз в большинстве случаев является обратимым процессом. Плазмолизированные клетки, помещенные в изотонический раствор, вновь набухают, восстанавливая свою жизнедеятельность. Но при слишком сильном и продолжительном обезвоживании клетка может потерять свою жизнеспособность.
При контакте с гипотоническим раствором вода из внешней среды переходит внутрь клетки. В результате этого увеличивается, и может произойти разрыв ее оболочки. Данное явление называется лизисом или эндосмосом (рис. 25).
Если в качестве клеточной культуры использовать эритроциты, то вследствие разрыва их оболочек внешняя среда окрасится гемоглобином в красный цвет. В этом случае данное явление называют иначе гемолизом (илиэритроцитолизом ).
Гемолиз является частным случаем более общего явления – цитолиза (разрушения животных и растительных клеток под влиянием различных причин).
В крови разрушение оболочки у всех эритроцитов наступает если ее осмотическое давление снижается до 260-300 кПа. Цвет крови при этом частично изменяется и принимает характерный, «лаковый» оттенок.
В клинической практике в некоторых случаях могут применяться не только изотонические, но и гипертонические растворы. Например, в хирургии используют марлевые полоски, смоченные в гипертоническом растворе NaClдля наложения на гнойные раны. При этом вследствие осмоса ток жидкости направляется по марле наружу из раны, что способствует постоянному очищению раны от гноя, микроорганизмов, продуктов распада и т.д. (рис. 26).

Рис. 26. Принцип применения гипертонических повязок для очистки пораженных тканей от гноя и продуктов распада
Гипертонические растворы вводят внутривенно при глаукоме, чтобы снизить внутриглазное давление из-за повышенного содержания жидкости в передней камере глаза.
Явлением осмоса объясняют слабительное действие глауберовой (Na 2 SO 4 · 10H 2 O) и горькой (MgSO 4 · 7H 2 O) солей.
Эти соли плохо всасываются в кровь и поэтому их высокая концентрация в кишечнике вызывает интенсивный переход воды внутрь него из окружающих тканей, способствуя послабляющему действию.
Многие бактериальные клетки имеют высокое осмотическое давление. При действии антибиотиков (например, пенициллина) ингибируется процесс биосинтеза стенок растущих стрептококков. Они становятся непрочными и под действием внутреннего осмотического давления легко разрушаются.
Таким образом, понимание и контроль осмотических процессов, а также умение оказывать на их протекание то или иное воздействие имеет крайне важное значение в биологии и медицине.